加州大学圣地亚哥分校的分子生物学家和生物工程师已经解开了衰老之谜背后的关键机制。他们分离出细胞在衰老过程中的两种不同路径,并设计了一种新的方法来通过基因编程来延长寿命。
这项研究发表在7月17日的《科学》杂志上。
我们人类的寿命是由我们个体细胞的老化决定的。为了了解不同的细胞是否以相同的速度和相同的原因老化,研究人员研究了发芽酵母的老化,这是一种研究老化机制的可操纵的模型,包括皮肤和干细胞的老化路径。
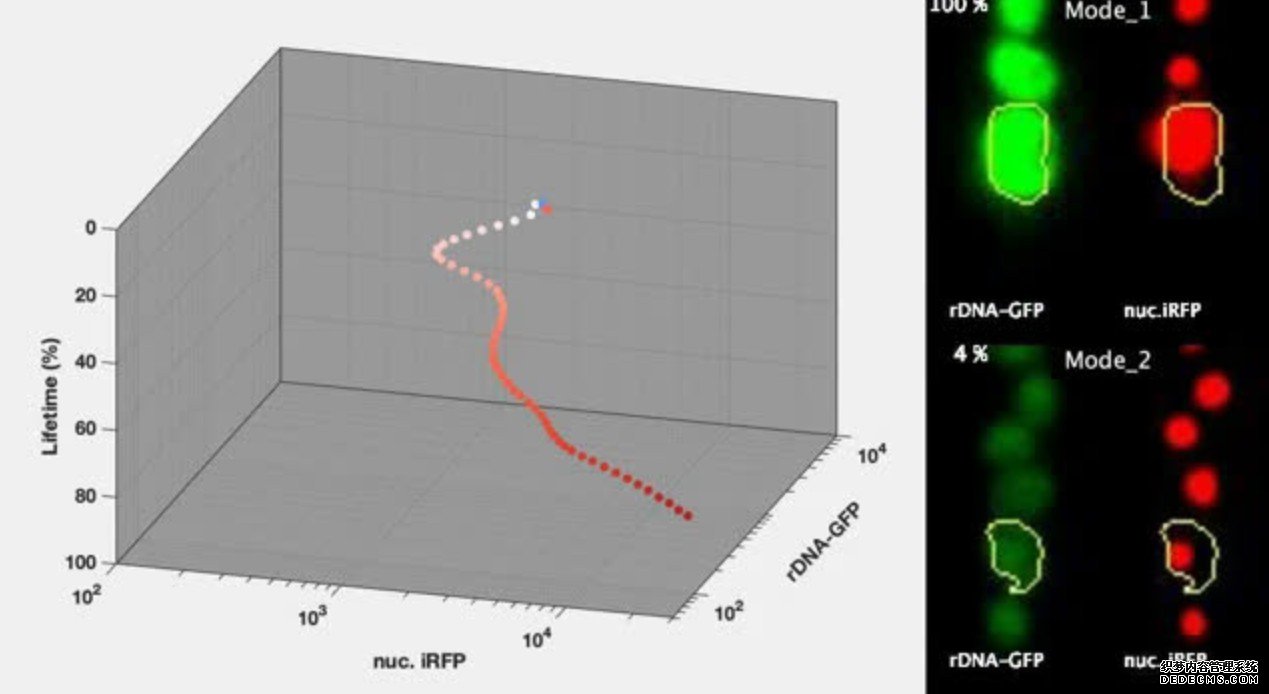
科学家们发现,具有相同遗传物质、处于相同环境中的细胞会以截然不同的方式衰老,它们的命运通过不同的分子和细胞轨迹展开。利用微流体、计算机建模和其他技术,他们发现大约一半的细胞随着核仁稳定性的逐渐下降而衰老。核仁是核DNA的一个区域,
登录杏耀手机客户端,蛋白质生产“工厂”的关键成分在这里合成。相比之下,杏耀注册另一半则是由于线粒体(细胞的能量生产单位)功能障碍而衰老。
在生命早期,细胞踏上了核仁或线粒体的路径,并在整个生命周期中通过衰老和死亡遵循这一“老化路径”。在控制中心,研究人员发现了一个引导这些老化过程的主电路。
“理解细胞如何做出这些决策,我们确定了分子老化过程底层每个路线和它们之间的联系,揭示分子电路控制细胞老化,类似于电路控制家用电器,“南郝说,该研究的资深作者的部分分子生物学副教授,生物科学分工。
郝和他的合作者们开发了一种新的老化景观模型,他们发现他们可以操纵并最终优化老化过程。计算机模拟帮助研究人员通过修改主分子电路的DNA,使他们能够创造一种新的以显著延长寿命为特征的老化途径。
郝说:“我们的研究提出了合理设计基因或化学疗法来重新编程人类细胞老化的可能性,我们的目标是有效地延缓人类衰老,延长人类健康寿命。”
研究人员现在将在更复杂的细胞和生物体中测试他们的新模型,并最终在人类细胞中寻找类似的衰老途径。他们还计划测试化学技术,并评估治疗和药物“鸡尾酒疗法”的结合可能如何引导长寿的途径。
“这篇论文的大部分工作都得益于一个强大的跨学科团队的组建,杏耀开户”分子生物学的生物科学教授Lorraine Pillus说,他是这项研究的合作者之一。“这个团队最重要的一点是,我们不仅要建模,还要进行实验,以确定模型是否正确。这些迭代过程对我们的工作至关重要。”





